Разложение этанола реакция. Этанол - что это? Свойства этанола
ОПРЕДЕЛЕНИЕ
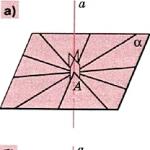
Этанол (этиловый спирт) — бесцветная легковоспламеняющаяся жидкость с алкогольным запахом (строение молекулы показано на рис. 1).
Он смешивается с водой во всех соотношениях и образует с ней азеотропные смеси (смеси определенного состава, кипящие при постоянной температуре, называют азеотропными смесями). Безводный этанол называют абсолютным спиртом, температура плавления которого составляет 78,37 o С.
Рис. 1. Строение молекулы этанола.
Таблица 1. Физические свойства этанола.
Получение этанола
В лабораторных условиях этанол получают следующими способами:
— гидролизом моногалогенпроизводных этана водными растворами щелочей
C 2 H 5 Br + NaOH aq →C 2 H 5 OH + NaBr (t o);
— гидрированием уксусного альдегида
CH 3 -C(O)H + H 2 → CH 3 -CH 2 -OH (kat = Ni, t o).
Основной промышленный способ получения этанола — гидратацияэталена:
CH 2 =CH 2 + H 2 O → CH 3 -CH 2 -OH (H + , t o).
Химические свойства этанола
Химические реакции, характерные для этанола сопровождаются расщеплением связей:
- взаимодействие с активными металлами
2C 2 H 5 OH + 2Na → 2C 2 H 5 ONa + H 2 .
- взаимодействие с органическими и кислородсодержашими неорганическими кислотами
C 2 H 5 OH + CH 3 COOH ↔ C 2 H 5 -O-C(O)-CH 3 + H 2 O (H 2 SO 4 (conc) , t o);
C 2 H 5 OH + HONO 2 ↔ C 2 H 5 ONO 2 + H 2 O (H 2 SO 4 (conc) , t o).
- взаимодействие с галогеноводородами
C 2 H 5 OH + HCl → C 2 H 5 Cl + H 2 O (ZnCl 2 , t o).
- взаимодействие с тригалогенидами фосфора
3C 2 H 5 OH + PBr 3 → 3C 2 H 5 Br + H 3 PO 3 .
- взаимодействие с аммиаком
C 2 H 5 OH + NH 3 → C 2 H 5 NH 2 + H 2 O (Al 2 O 3 , t o = 300).
3) O-H и C α -H;
- дегидрирование
CH 3 -CH 2 -OH → CH 3 -C(O)H + H 2 (kat = Cu, t o).
- окисление
CH 3 -CH 2 -OH + 2[O] → CH 3 -COOH + H 2 O (kat, t o).
4) C-OH и C β -H
- внутримолекулярная дегидратация
CH 3 -CH 2 -OH → CH 2 =CH 2 + H 2 O (Al 2 O 3 , t o).
Применение этанола
Основное направление использование этанола - промышленный органический синтез. Кроме этого он применяется в фармации для приготовления настоек и экстрактов, а также в медицинской практике - как наружное антисептическое средство для дезинфекции рук и хирургических инструментов.
Примеры решения задач
ПРИМЕР 1
ПРИМЕР 2
| Задание | Напишите уравнения реакций, с помощью которых можно осуществить превращения:
Этилен → Этанол → Диэтиловый эфир → Иодоэтан → Бутан. Укажите условия протекания реакций. |
| Ответ | В присутствии серной кислоты алкены способны присоединять молекулы воды. В результате подобной реакции из этилена можно получить этанол:
CH 2 =CH 2 + H 2 O →C 2 H 5 OH. Спирты способны подвергаться межмолекулярной дегидратации в результате чего происходит образование простых эфиров. Данная реакция протекает под действие водоотнимающих реагентов, например, серной кислоты: C 2 H 5 OH + HOC 2 H 5 → C 2 H 5 -O-C 2 H 5 + H 2 O. При действии иодоводорода на диэтиловый эфир в кислой среде происходит его расщепление на иодоэтан и этанол: C 2 H 5 -O-C 2 H 5 + HI → C 2 H 5 OH + C 2 H 5 I. Получение бутана из иодоэтана возможно по реакции Вюрца 2 C 2 H 5 I + 2Na → CH 3 -CH 2 -CH 2 -CH 3 + 2NaI. |

Этиловый алкоголь почти полностью всасывается из желудка и тонкой кишки в систему воротного кровообращения и быстро достигает печени. Около 95% введенного в организм алкоголя окисляется в печени, остальные 5% в неизменном виде выделяются с мочой и с выдыхаемым воздухом. Таким образом, печень является единственным органом, способным эффективно избавлять организм от избытка этанола. Скорость превращения этанола в печени до конечных продуктов - и воды составляет 0,1 г чистого алкоголя на 1 кг массы тела в час, т. е. около 7-8 г в час. Таким образом, печень взрослого человека с массой в 70-80 кг при максимальном напряжении своих метаболических способностей может обезвредить до 180 г алкоголя, выработав при этом около 1400 ккал.
В печени этанол сначала превращается в уксусную кислоту (ацетат), которая, соединяясь с коэнзимом А, образует ацетил-коэнзим А. Далее в составе ацетил-коэнзима А окисляется в цикле Кребса до углекислоты и воды.
Обмен алкоголя в печени осуществляется несколькими ферментными системами, из которых основную роль играет система алкогольной дегидрогеназы (АДГ) в цитозоле печеночной клетки. Наличие АДГ в печени человека объясняется тем, что небольшие количества алкоголя вырабатываются в нормальных условиях бактериями тонкой кишки. Распад алкоголя в печени проходит через несколько этапов (рис. 17). Первоначально под влиянием АДГ этанол окисляется до также весьма токсичного промежуточного продукта - ацеталь- дегида с высвобождением водорода. Коферментом этой реакции является НАД. Присоединяя отщепившийся от молекулы этанола водород, НАД восстанавливается в НАДН (восстановленный НАД):
СН 3 СН 3 ОН+НАД ↔ СН 3 СНО+НАДН+Н + (1)
Образующийся ацетальдегид в свою очередь окисляется в митохондриях гепатоцита до уксусной кислоты (ацетата) при участии ацетальдегиддегидрогеназы (АЦДГ). Коферментом этой реакции также является НАД:
СН 3 СНО+НАД ↔ СН 3 СООН+НАДН (2)
Более 90% ацетата в составе ацетил-коэнзима А далее окисляется в цикле трикарбоновых кислот Кребса и в дыхательных цепях митохондрий до углекислоты и воды.
В обеих оксилительных реакциях (1,2) расходуется НАД и образуется накапливающийся в печени НАДН. В результате соотношение НАДН:НАД в клетке печени увеличивается. Длительное изменение этого соотношения при окислении больших количеств алкоголя приводит к значительному снижению окислительно-восстановительной способности печени и оказывает неблагоприятное влияние на течение многих обменных процессов в гепатоците, особенно на обмен жиров и .

Рис. 17. Схема окисления в печени
Повышенное образование ацетил-коэнзима А при окислении больших количеств алкоголя приводит к увеличению синтеза жирных кислот, продуцируемых этим соединением, а при накоплении в печени НАДН снижается скорость их окисления в митохондриях гепатоцита. Кроме того, реокисление НАДН в НАД идет в основном по пути образования гепатоцитом из водорода и ацетил-коэнзима А жирных кислот. Активация цикла Кребса в ходе расщепления этанола приводит к повышению синтеза глицерина в форме α-глицерофосфата, который активно реагирует с жирными кислотами, образуя нейтральный жир (триглицериды). Повышению количества жирных кислот в печени способствует также повышенное их поступление из жировой ткани, где жирные кислоты высвобождаются в результате липолиза - распада нейтрального жира при стимуляции высокими дозами алкоголя симпатической нервной системы. В результате этих нарушений обменных процессов создаются все предпосылки для синтеза в печени из накапливающихся жирных кислот и глицерина жира. Содержание нейтрального жира в печени при алкогольной жирной печени увеличивается в 3-12 раз. Этому способствует затруднение удаления избыточного жира из печени из-за снижения продукции печенью липопротеинов (сложных комплексов липидов с белками, в форме которых осуществляется транспорт жиров и из печени в кровь).
Важным следствием увеличения соотношения НАДН:НАД является уменьшение окисления в печени образуемой в мышцах при их работе из глюкозы молочной кислоты (лактата). Печень в норме снова превращает лактат в глюкозу и гликоген при участии АТФ в процессе глюконеогенеза (новообразования глюкозы). Алкоголь тормозит этот процесс, так как избыток НАДН реокисляется в НАД, не только в митохондриях, но и в печеночной клетки ферментативной системой, которая в норме превращает молочную кислоту в пировиноградную. В результате возможно значительное обеднение печени гликогеном, особенно если введение больших доз алкоголя сочетается с голоданием. При истощении запасов гликогена в печени уровень глюкозы крови после очередного алкогольного эксцесса может резко снижаться - развивается тяжелая, угрожающая жизни, гипогликемия с судорогами и потерей сознания. Вместе с тем у 2/3 больных алкоголизмом обнаруживается сахарный диабет, особенно при избытке в диете углеводов.
Страницы: 1
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
ФАРМАКОПЕЙНАЯ СТАТЬЯ
Спирт этиловый 95%, 96 % ФС.2.1.0036.15
Этанол Взамен ВФС 42-2761-96;
Ethanolum в замен ФС 42-3072-00
С 2 Н 6 О М. м. 46,07
Спирт этиловый 95% содержит от 94,9 % до 96,0% этанола С 2 Н 6 О (о/о), от 92,3% до 93,8% (м/м); спирт этиловый 96% содержит от 95,1% до 96,9% этанола (о/о), от 92,6% до 95,2% (м/м).
Настоящая фармакопейная статья распространяется на спирт этиловый 95% и спирт этиловый 96 %, вырабатываемый из различных видов сахар- и крахмалосодержащего пищевого сырья и применяемый для производства/изготовления стерильных и нестерильных лекарственных форм.
Описание
Прозрачная бесцветная подвижная жидкость с характерным спиртовым запахом.
Растворимость
Смешивается с водой, хлороформом, ацетоном и глицерином во всех отношениях.
Подлинность
- Качественная реакция. 2 мл субстанции смешивают с 0,5 мл уксусной кислоты ледяной и 1мл серной кислоты концентрированной и нагревают до кипения; должен появиться характерный запах этилацетата.
- Качественная реакция. 0,5 мл субстанции смешивают с 5 мл 10 % раствора натрия гидроксида, прибавляют 2 мл 0,05 М раствора йода; должен появиться запах йодоформа и постепенно образоваться желтый осадок.
Плотность
Спирт этиловый 95%: от 0,808 до 0,812 г/см 3 (при 20 о С, ОФС «Плотность).
Спирт этиловый 96%: от 0,804 до 0,811 г/см 3 (при 20 о С, ).
Прозрачность
Смесь равных объемов субстанции и воды должна быть прозрачной ().
Цветность
Субстанция должна быть бесцветной ( , метод 2).
Кислотность или щелочность
К 20 мл субстанции прибавляют 25 мл свежепрокипяченной и охлажденной воды и 0,1 мл 1 % раствора фенолфталеина. Раствор остается бесцветным и окрашивается в розовый цвет, устойчивый в течение 30 с, при прибавлении не более 0,2 мл 0,05 М раствора натрия гидроксида.
Хлориды
Микробиологическая чистота
В соответствии с ОФС «Микробиологическая чистота.
Хранение
В плотно укупоренной упаковке, вдали от огня.
 Как бы парадоксально ни звучало, но прогресс не всегда давал только положительный эффект. Например, различные настои на спирте изначально появились и использовались, как лечебные. А сам спирт — как консервант для веществ, имеющихся в плодах и ягодах.
Как бы парадоксально ни звучало, но прогресс не всегда давал только положительный эффект. Например, различные настои на спирте изначально появились и использовались, как лечебные. А сам спирт — как консервант для веществ, имеющихся в плодах и ягодах.
Где-то в середине XV века русские нашли технологию получения спирта на основе собственного сырья. После войны с Наполеоном 1812 года русскую водку во Франции стали воспринимать, как благородный и чистый напиток победителей.
О вреде, а возможно и пользе, употребления алкоголя рассказывается в видео материале.
Видео-урок «Спирт в организме человека»
На фоне эйфории прогрессирующих масштабов, популярности и разнообразия напитков, специалисты стали все чаще задумываться над такой проблемой, как влияние спирта на организм. И прежде всего, что такое этиловый спирт?
Ответ прост — это химическое соединение, вредное для организма.
Очень малая часть его при употреблении всасывается во рту. Около 80%- в тонком кишечнике и примерно пятая часть — в желудке. Разложение спирта в организме человека, происходит вдоль всего пути похождения алкоголя:
- Спирт попадает в организм.
- Опускается в желудок.
- В желудке начинается переработка спирта.
- Спирт попадает в сердце.
- Сердце поставляет спирт в головной мозг.
Печень содержит основные ферменты, которые ведут расщепление спирта. Более того, организм тоже вырабатывает алкоголь, всего лишь 0,01%. Но этого достаточно, чтобы обеспечить 10% объема энергетического обмена веществ.
Много это или мало?
Если человек выпил стакан водки, через несколько часов в организме появится дополнительная порция алкоголя: 80кг (вес) + 200г (водка) + 2 часа = 0,1% эндогенного алкоголя.
Обратите внимание на разницу между 0,1%, которые попадают извне с водкой, без всякого труда, и 0,01%, которые вырабатывает сам организм? Это все равно, что человеку, работающему с одной лопатой, дать в помощь еще 10 человек с лопатами. Что станет делать первый? Он перестанет работать и начнет постоянно требовать помощи извне.
Еще сложнее ситуация с женским организмом, у которого отсутствуют необходимые ферменты, в частности, в желудке.
Второй фермент, который включает действие организма при появлении в нем алкоголя, находится в клетках организма человека.
Печень и почки наиболее активны в противодействии алкоголю. А сердечная мышца, головной мозг и сетчатка глаза, как его часть, защищены в меньшей степени- это самое слабое звено в цепочке продвижения алкоголя по организму. Но здесь образуется наибольшая концентрация спирта: в головном мозге она выше, чем в крови в полтора раза, поэтому и действие алкоголя ощутимее.
Разложение спирта в организме человека из своего опасного состояния, С2Н5ОН, проходит через превращение в еще более опасное соединение ацетальдегид — СН3СНО и ацетил коэнзим А,СН3СООН, и только после этого в воду, Н2О, и углекислый газ, СО2.
Выведение токсических веществ из организма — главный вопрос для понимания процесса, как лечить.
Проблема не только в водке, а и в дозировке. Наши «профессионалы застолья» высмеивают сюжеты заморских фильмов, где герои весь вечер маленькими дозами пьют бокал пива. Но это вовсе не от слабости. Киногерои в кадре, как раз употребляют столько алкоголя, сколько организм человека может справиться.
Определена норма, которую нельзя превышать
Каждые 1-2 грамма на 1 кг веса человека безвредны для организма или:
- 40-60 или, максимум, 80 мл водки;
- бокал вина, т.е. 150 – 200 мл;
- 0,3 литра пива.
Желаем здоровья и разумного пития во время застолий!